Door het verbranden van kolen, aardolie en aardgas neemt de hoeveelheid CO2 in de lucht langzaam maar zeker toe. Omdat CO2 een broeikasgas is, warmt de aarde hierdoor langzaam op. Al die extra CO2 blijft niet in de lucht, maar een groot gedeelte lost op in de bovenste laag van het zeewater: deze uitwisseling en de verdere verplaatsing door zeestromingen heten samen ook wel de 'solubility pump' (NL: oplosbaarheidspomp, ofwel het rondvoeren van de “opgeloste” CO2) en is een puur natuurkundig proces. Zodoende is ongeveer 25% van de uitgestoten CO2 opgenomen door de oceanen. Omdat deze opgeloste CO2 reageert met water en daarmee koolzuur vormt, verzuurt de oceaan langzaam. Dit staat ook wel bekend onder de Engelse term ‘Ocean Acidification’, oftewel oceaanverzuring.
Verzuring is in feite een toename van de concentratie van protonen (H+ ionen). Ook wordt dit wel uitgedrukt met de pH schaal: hoe hoger de concentratie H+, hoe lager de pH van water. En omdat deze schaal logaritmisch is (net als bijvoorbeeld de schaal van Richter of decibellen), betekent een verlaging van de pH met 1, dat de concentratie H+ tien keer zo hoog wordt (Figuur 1). De gemeten daling in de pH van 0,1 lijkt dus misschien klein, maar dat betekent dat de concentratie H+, en dus de zuurgraad van het zeewater met 25% is toegenomen.
Zonder biologische activiteit zou enkel de ‘solubility pump’ werken en bepalen hoeveel CO2 er tussen de lucht en de zee wordt uitgewisseld. De opname door oplossing in de bovenste laag van de oceanen is nu ongeveer 3 gigaton (=3 × 1012 kg) koolstof per jaar. Die drie gigaton is langzaam toegenomen in de loop van de tijd: in 1960 was de opname nog ongeveer 1 gigaton [1]. Ter vergelijking: 1 gigaton is gelijk aan het gewicht van ongeveer 200 miljoen olifanten.
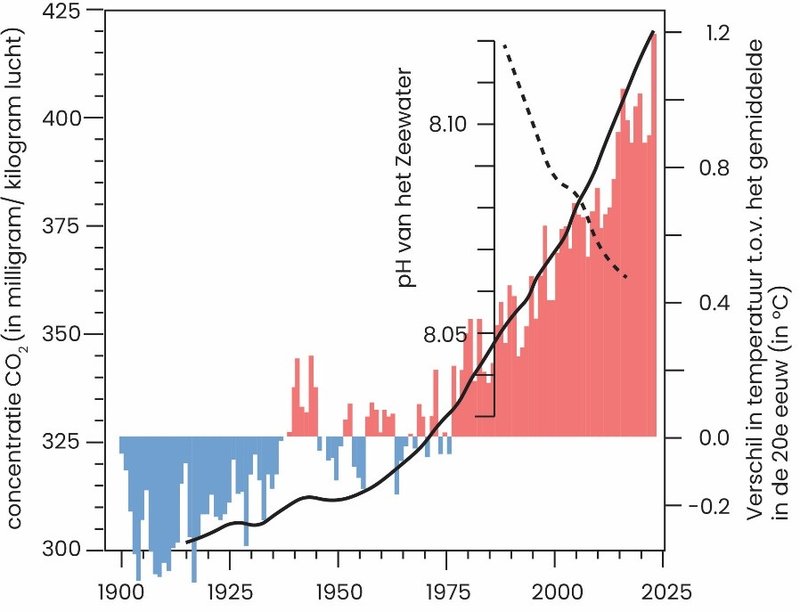
Figuur 1: De toename in de gemiddelde temperatuur op aarde (in blauw en rood) als gevolg van de toenemende concentratie van CO2 in de lucht (zwarte lijn). Het stippellijntje rechtsboven geeft de daling in pH (toenemende zuurgraad) die het gevolg is van de toenemende CO2 concentratie.
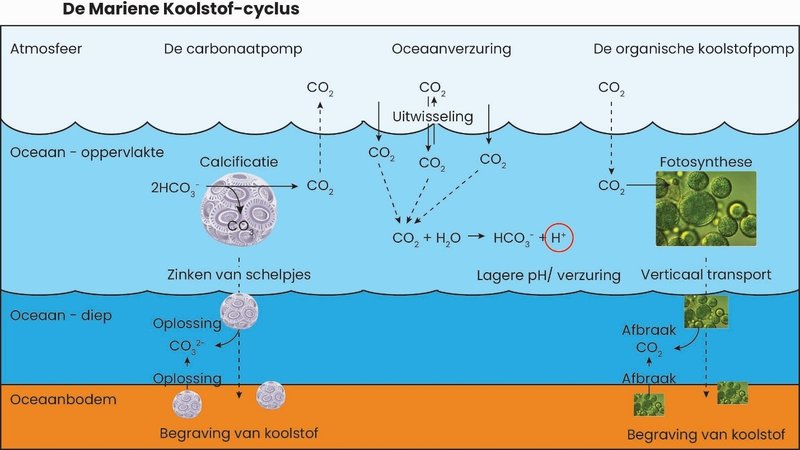
Naast de solubility pomp zijn er in de open oceaan zijn er twee belangrijke, biologische processen die beïnvloed worden door opgelost CO2 (figuur 2). Fotosynthese door algen neemt CO2 op en legt dat vast als organisch koolstof: dat zijn in dit geval de cellen van de algen. Dit werkt net zoals planten op het land. In totaal wordt er op deze manier ongeveer 50 gigaton aan koolstof vastgelegd in de bovenste laag van de oceaan [2]. Net als blaadjes van bomen worden de meeste algen weer afgebroken waarbij het opgenomen CO2 weer vrij komt. Slechts ongeveer 20% (10 gigaton) van de algen zinkt richting diepere waterlagen. Daarvan wordt nog eens 80% (8 gigaton) afgebroken voordat het neerkomt op de oceaanbodem. Van de 2 overgebleven gigaton wordt nog eens 90% afgebroken. Uiteindelijk wordt ongeveer 0.2 gigaton begraven in het sediment. Het proces van koolstof dat in de vorm van CO2 uit de atmosfeer op deze manier naar de diepzee wordt getransporteerd wordt ook wel de ‘organische koolstofpomp’ genoemd. Zodra de koolstof naar de diepe oceaan zinkt zijn we het even kwijt. Het duurt, afhankelijk van de plek waar dit gebeurt, gemiddeld een paar eeuwen voordat het door oceaanstromingen weer terugkomt naar het oppervlak. Dit proces dempt dus de stijging van de CO2 concentratie door de mens.